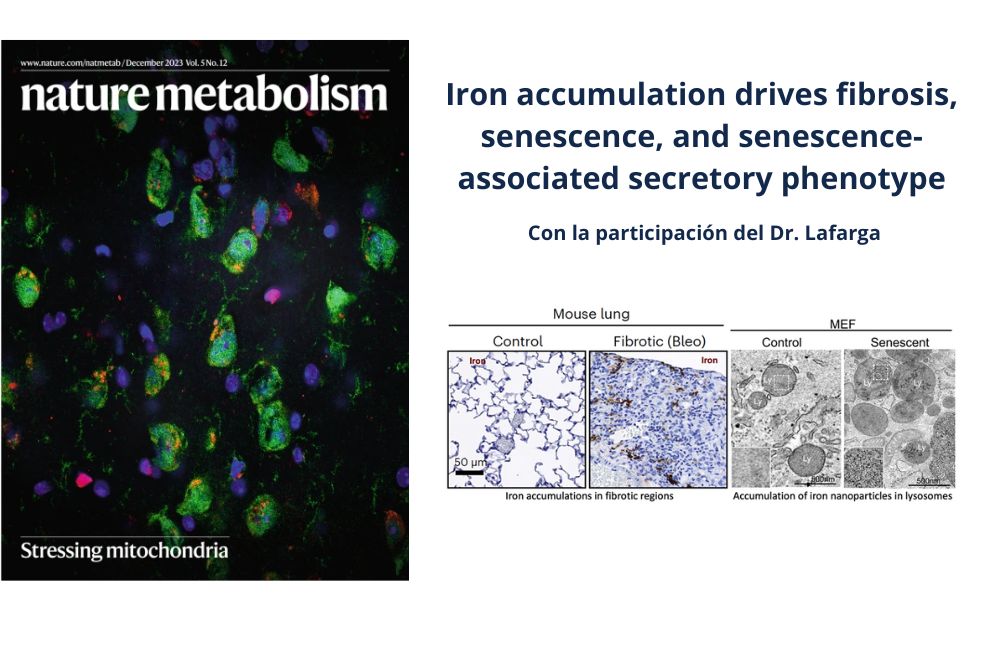
El Dr. Miguel Lafarga participa en este estudio internacional publicado en la prestigiosa revista Nature Metabolism
Las enfermedades fibróticas afectan al normal funcionamiento de los órganos y representan el 45% del total de la mortalidad de los países desarrollados. La fibrosis se asocia con diversas afecciones crónicas y potencialmente mortales, como la fibrosis pulmonar, la cirrosis hepática, así como las enfermedades renales y cardiovasculares, entre otras.
El Dr. Miguel Lafarga, investigador del Grupo Biología Celular del Núcleo de IDIVAL y Profesor Emérito de la Universidad de Cantabria (Departamento de Anatomía y Biología Celular) ha participado en una investigación internacional que plantea un nuevo enfoque en la concepción de las enfermedades fibróticas.
Los resultados de este estudio “Iron accumulation drives fibrosis, senescence, and senescence-associated secretory phenotype” han sido publicados recientemente en la prestigiosa revista científica Nature Metabolism. Una investigación liderada por el Dr. Manuel Serrano, “Altos Labs” (Cambridge, UK), y financiada con proyectos de la Unión Europea (Horizon 2020 y European Research Council).
Los investigadores han estudiado el vínculo entre la acumulación de hierro, la senescencia (una fase en la que las células no se dividen ni mueren) y el fenotipo secretor asociado a la senescencia (SASP). Un trabajo multidisciplinar que combina ciencias ómicas, bioquímica, histoquímica, microscopía electrónica y MRI, realizado in vitro y en modelos experimentales de ratones con fibrosis pulmonar, renal o cardíaca, así como en pacientes con nefropatía diabética y distress respiratorio agudo.
“La activación de la fibrogénesis es un mecanismo fisiológico de respuesta a la lesión de los tejidos, pero si se hace irreversible y progresiva da lugar a graves enfermedades fibróticas” explica el Prof. Lafarga. Esta investigación demuestra que la acumulación de hierro extracelular, por ejemplo, en lesiones vasculares y hemolíticas, puede tener un potente efecto profibrótico en los tejidos circundantes mediante la activación de un programa de senescencia celular. Las células senescentes no se dividen ni se mueren, pero secretan moléculas potencialmente dañinas, un mecanismo conocido como “fenotipo secretor asociado a la senescencia (SASP)”. Las células senescentes acumulan hierro de forma persistente, principalmente en los lisosomas, que activa el SASP y la fibrosis, explica el Dr. Lafarga.
El metabolismo del hierro como diana terapéutica para detener la fibrosis
Los investigadores identifican el metabolismo del hierro como un objetivo terapéutico potencial para las enfermedades asociadas a la senescencia. En particular, el uso de agentes químicos capaces de eliminar los acúmulos de hierro e inhibir la actividad profibrótica del SASP, como la deferiprona -un fármaco aprobado para la prevención de la fibrosis-, abre un nuevo horizonte en el tratamiento de enfermedades fibróticas.
Los autores también demuestran que la detección de hierro mediante resonancia magnética podría permitir una valoración diagnóstica no invasiva de la carga fibrótica en los riñones de ratones y en pacientes con fibrosis renal.
Los resultados de esta investigación revelan un importante avance y un cambio de paradigma en el conocimiento de la fisiopatología de las enfermedades asociadas a la senescencia y envejecimiento que cursan con fibrosis. Un problema crítico de salud que requiere más investigaciones y estudios clínicos.
Ref: Iron accumulation drives fibrosis, senescence, and senescence-associated secretory phenotype”. Mate Maus, Vanessa Lopez-Polo, Lidia Mateo, Miguel Lafarga, Monica Aguilera, Eugenia De Lama, Kathleen Meyer, Anna Sola, Cecilia Lopez Martinez, Ines Lopez-Alonso, Marc Guasch-Piqueras, Fernanda Hernandez-Gonzalez, Selim Chaib, Miguel Rovira, Mayka Sanchez, Rosa Faner, Alvar Agusti, Rodrigo Dieguez Hurtado, Sagrario Ortega, Anna Manonelles, Stephan Engelhardt, Freddy Monteiro, Camille Stephan-Otto Attolini, Neus Prats, Guillermo Albaiceta, Josep M. Cruzado & Manuel Serrano. Nature Metabolism (2023) DOI: 10.1038/s42255-023-00928-2